电化学(2):电位法
电位法是电化学方法中一种常用的方法,基于原电池(Galvanic Cell)的原理。电位法应用场景包括pH值测量,临床血气分析,市政污水污染物监测,海水中二氧化碳含量检测等。

电势法是在不产生明显电流的情况下测量电化学电池(原电池)的电位,通过电位来分析目标物质的浓度。电位测定法的设备简单且便宜,包括参比电极、指示电极和电位测量装置。
基本原理
对于下图所示的原电池,电位的计算公式为:
$$E_{cell} = E_{ind} - E_{ref} + E_j$$
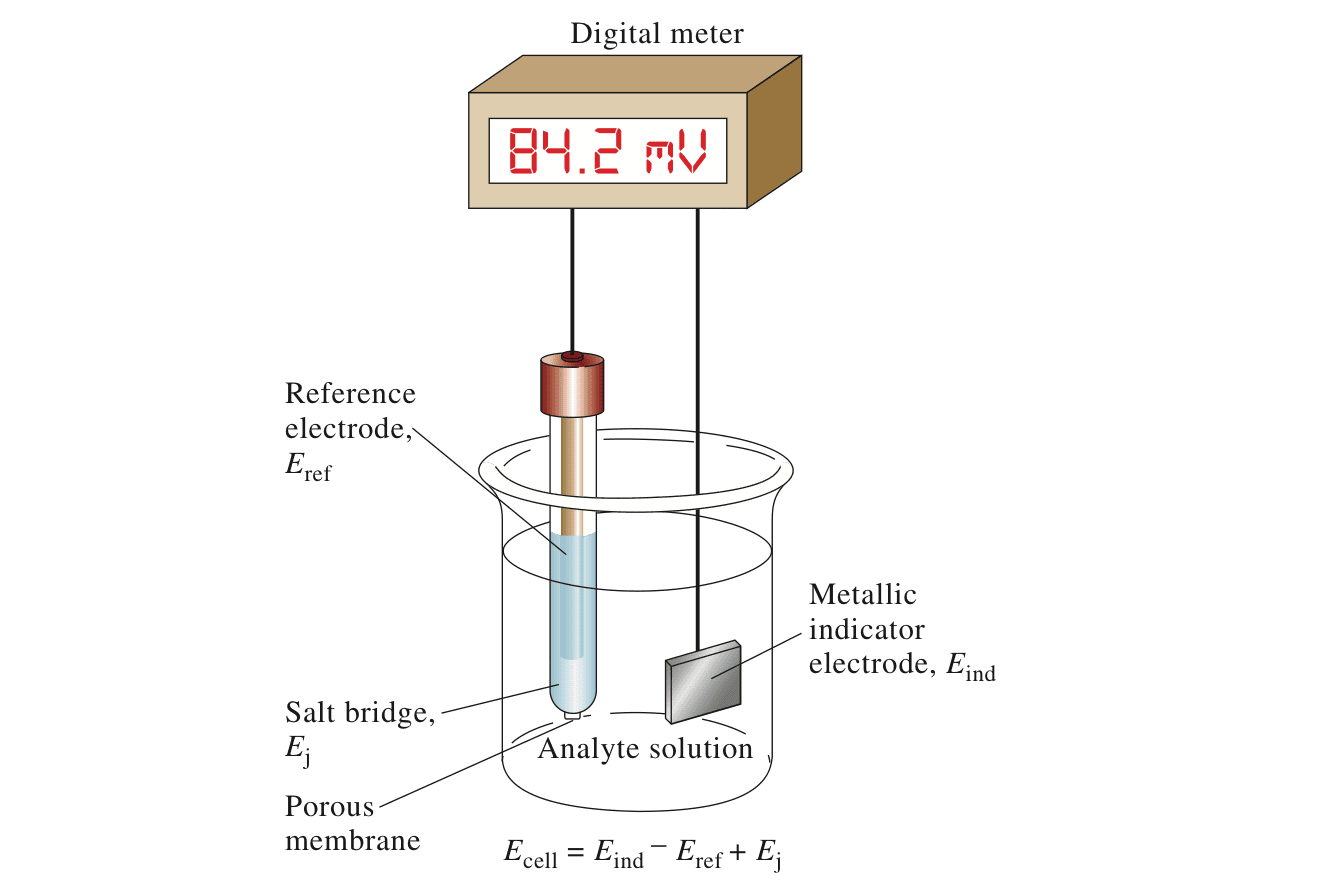
- $E_{ref} $为参考电极(Reference Electrode)的电势。参考电极必须提供一个稳定的电势,而且不受目标物质浓度的影响。参考电极可以是《电化学基础》里提到的标准氢电极,但因制造复杂而比较少用。
- $E_{ind}$为指标电极(Indicator Electrode)的电势。
- $E_j$为盐桥电势。盐桥可以防止分析物溶液的成分与参比电极的成分混合。
以上便是电位法的三个重要组成部分。指示电极的电位与目标物质的浓度有关系。通过设计稳定的参比电势,然后通过指示电极的电位计算出目标物质的浓度。
参比电极
理想的参比电极具有精确已知、恒定且对分析物溶液的组成完全不敏感的电势。此外,该电极应坚固耐用,易于组装,并应在通过最小电流的同时保持恒定的电势。参比电极有:标准氢电极(SHE)、甘汞电极、银|氯化银电极等。市场最广泛的参比电极系统由浸入饱和氯化银和饱和氯化钾溶液中的银电极组成。下图是示意图:
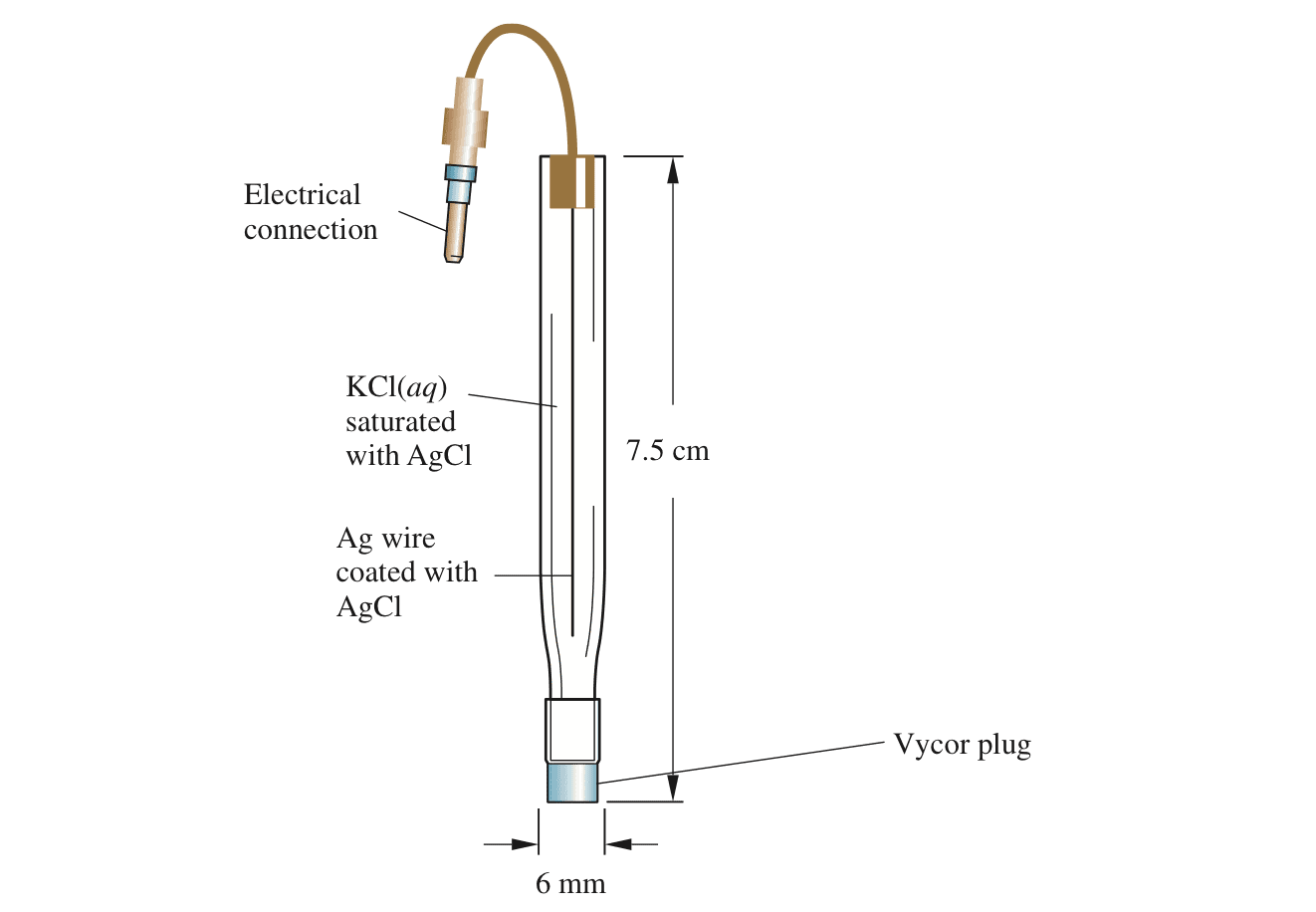
指示电极
理想的指示电极可对目标分析离子浓度的变化做出快速且可重复的响应。 指示电极有三种类型:金属电极(Metalic)、膜电极(Membrane)和离子敏感场效应晶体管(ion-sensitive Field Effect Transistor)。不同电极的设计不一样,这里只介绍最常见的电极是膜电极,应用于测量pH、离子、水中气体等。
膜电极也称为离子选择电极(ion-selective electrode, ISE),膜电极与参比电极组成下图所示的电化学原电池。参比电极的电势是恒定的,因此在指示电极的电势情况包含关于样品中分析物量的信息。由于膜具有选择性,只能通过特定的离子或其它物质,膜电极在测量方面也具有选择性。
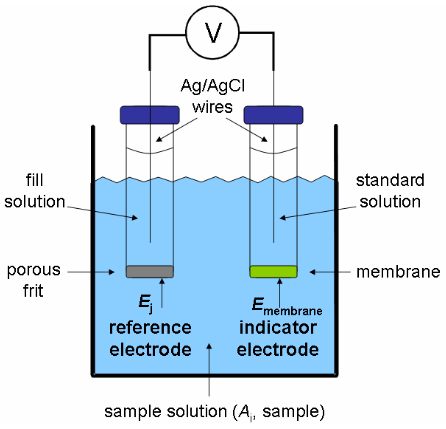
理想的膜电极(离子选择电极)包含一层只有特定的离子可以穿过的薄膜。 在薄膜两侧,离子从高浓度到低浓度的传输会产生电位差(Concentration Cell)。根据膜材料,膜电极(离子选择电极)可分为以下四种类型:
- 玻璃膜电极(Glass membrane electrode)
- 固态膜电极(Solid state membrane electrodes)
- 液膜电极(Liquid membrane electrode)
- 气体感应电极(Gas sensing electrode)